Salzwasser-Elektrolyse?
Ich verstehe einfach mich, wie die Salzwasser-Elektrolyse chemisch abläuft. Warum wird Wasserstoff gewonnen? Dann müsste doch genau so gut Sauerstoff gewonnen werden, wenn das Hydroxid-Ion die Elektronen abgibt. Kann mir jemand es einfach chemisch erklären? Ich verstehe halt nicht, wie die Elektronen von der Kathode zur Anode kommen.
2 Antworten
Wasser nennt man H2O.Wasser besteht also aus Wasserstoff und Sauerstoff. Bei der Elektrolyse wird das Wasser aufgespaltet in Wasserstoff und Sauerstoff. Am Minuspol entsteht Wasserstoff und am Pluspol Sauerstoff.
Wasser besteht aus: 2 Teilen Wasserstoff und 1 Teil Sauerstoff
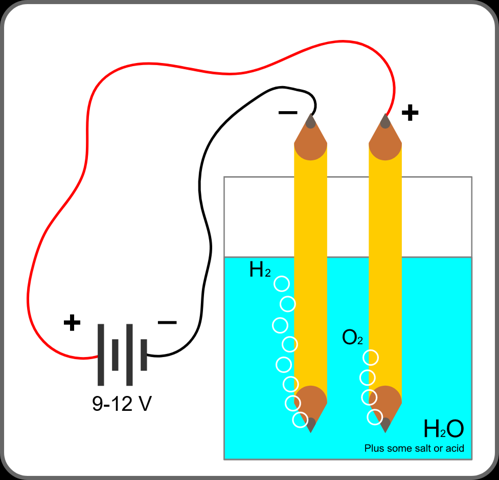
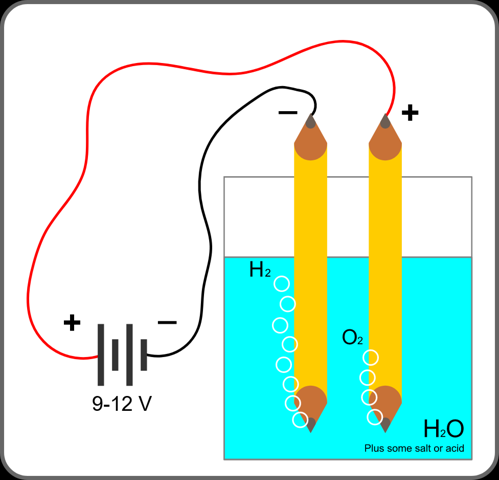
Wieso muss man übrigens nach einer Weile NaCl nachfüllen? Passiert damit während der Elektrolyse auch etwas?
Ich verstehe es auch nicht. Und als ich es mal versuchte, hat's auch nicht funktioniert. Es blubbert zwar an der Anode, aber das ist wohl eher das Chlorgas vom Kochsalz.
Was Wasser ist weiß ich natürlich. Ich verstehe nur nicht, wie der Strom im Salzwasser übertragen wird. Wo werden die Elektronen transportiert. Und warum entsteht nur Wasserstoff, jedoch kein Sauerstoff, obwohl bei der Wasser-Elektrolyse Sauerstoff entsteht. Also muss es ein Unterschied bei der Elektrodenübertragung zwischen Kathode und Anode geben.