Lewis Formel von Thiosulfat S2O3 ^2-
Hallo :) Ich soll die Lewis-Formel von S2O3 ^2- zeichnen und hab das mehr oder weniger hingekriegt. Hab aber einen Fehler gemacht. Nämlich eine Doppelbindung zwischen den S-Atomen und die zweite Doppelbindung zwischen S- und O-Atom (siehe Bild) gezeichnet. D.h., dass die negative Ladung in meiner Variante bei zwei Sauerstoffatomen liegt. Die Lösungen sehen leider etwas anders aus. Nämlich liegen die Doppelbindungen nur zwischen S- und O-Atomen, so dass ein Schwefelatom auch eine negative Ladung hat. Nun wollte ich fragen, ob meine Variante falsch ist und weshalb?
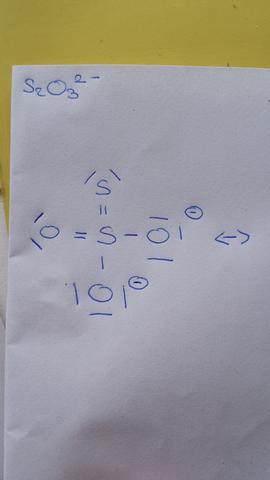
2 Antworten
Der neueren Ansicht, dass es gar keine Oktettüberschreitung gibt, entspräche, dass überhaupt nur Einfachbindungen vorkommen. Demzufolge wären alle O und der äußere S negativ, der zentrale S zweifach positiv partialgeladen. Die Wahrheit liegt wohl dazwischen, mit Sicherheit liegt ein mesomeriestabilisiertes Ion vor, für das man allerlei Grenzformeln zeichnen kann.
Wegen der EN-Differenz zwischen O und S ziehen die Sauerstoffe bevorzugt Elektronen zu sich um die Edelgaskonfiguration zu erreichen. Da hat der Schwefel dann das Nachsehen.
Mit einer negativen Ladung hat der Schwefel dann ja mehr Elektronen als ein Sauerstoffatom?