Gibt es so eine Wasserstoffbrückenbindung?
Hey,
ich habe 2 Frage zur organischen Chemie und zwar
- Kann es diese Wasserstoffbrückenbindung geben und was würde man als Produkte erhalten? Und sind die Partialladungen richtig dargestellt?
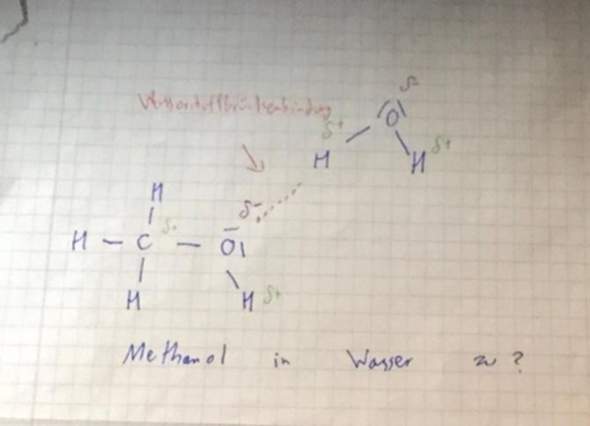
2.Kann Essigsäure mit Wasser reagieren und welche Ausgangsprodukte gibt es dann? Und ist die Darstellung der Partialladungen korrekt?
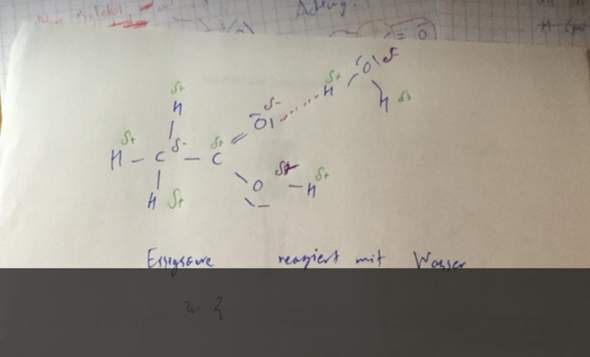
Danke sehr für die Antwort
VG
MrJam9
2 Antworten
1) Ja, das ist alles richtig. Auch die WBB. Es gibt allerdings noch eine zweite WBB vom rechten H des Methanol zum O vom Wasser. Ansonsten passiert da nichts.
2) Es kommt zur Protonenübertragung: Das rechte H der Essigsäure bindet sich an ein freies EP vom H2O. So entstehen H3O+ und ein Acetatanion. Die Ladungen sind soweit ok. Die Ladungen am linken Methylteil der Essigsäure sind aber nur schwach und heben sich gegenseitig auf. Die würde man eigentlich nicht zeichnen.
LG
Zu 1: Ja diese Wasserstoffbrücke gibt es. Ein Produkt kommt dabei nicht raus. Ist das Gleiche, wie wenn du einen Alkohil in Wasser löst. Kommt auch kein Produkt raus.
Zu 2: Essigsäure kann protoniert und deprotoniert werden. Das heißt, weil Wasserstoff H3O+ unh OH- Ionrn produziert, dürften ständig auch minimale Wechselwirkungen mit Essigsäure und den obigen 2 Ionen enstehen, sodass man manchmal eine coo- Gruppe erhalten dürfte.