[Chemie] Warum besteht Metall aus Ionen?
Guten Morgen,
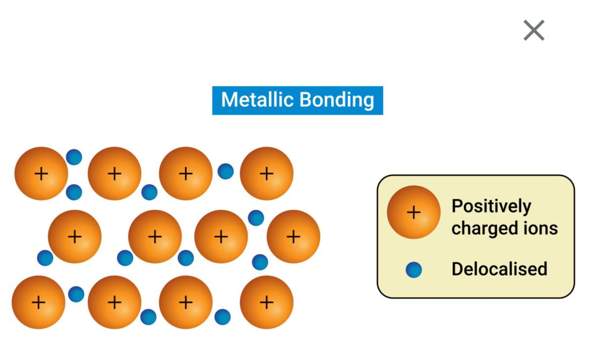
warum besteht Metall aus positiv geladenen Ionen? Das es die Elektronengase gibt, weiß ich. Aber wieso handelt es sich um positiv geladene Ionen?
3 Antworten
So ein Block Metall ist natürlich elektrisch neutral. Da die negativ geladenen Elektronen als Gas quer durch den Block schwirren, muß irgendwo die ausgleichende positive Ladung herumhängen. Nämlich bei den Metallatomen, die ihre Elektronen an das Band abgegeben haben.
Die Metallatome sind also von ihren Elektronen getrennt, und wenn man will, dann kann man sie als Ionen bezeichnen. Natürlich sind das nicht im selben Sinn Ionen wie bei einem Salz, weil sie von den Elektronen nicht vollständig getrennt sind (es schwirren ja immer wieder welche vorbei). Manchmal nennt man sie daher auch „Atomrümpfe“, um sie begrifflich von den Ionen in einem Salz zu unterscheiden.
Der Begriff Ion ist hier definitiv falsch und wie du gerade selbst merkst, irreführend.
In der Metallbindung schwingen die positiven Atomrümpfe auf festen Gitterplätzen und sind dabei von Elektronen"gas" umgeben.
Dadurch sind die wesentlichen Metalleigenschaften erklärbar: Die Schwingungen reiben am Nachbar, was zur Wärmeleitung führt, das freie Elektronengas leitet Strom und die Verschiebung der gesamten Gitterebenen ist die Verformbarkeit.
Aber definitiv nix mit Ionen.
m.f.G.
anwesende
Weil bei Ionen die negativ geladenen Elektronen gerade auf Wanderschaft und nicht da sind.