Wie entsteht das Dithionit-Ion und was passiert bei der Reaktion von Wasser und Natriumdithionit?
Hallo,
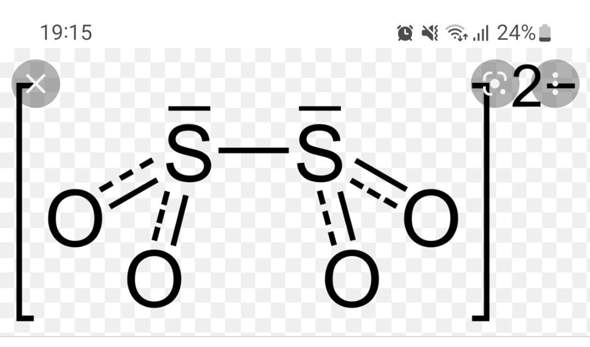
Wo genau finde ich im Dithionit-Ion die zwei "zu vielen" Elektronen? Ich verstehe den Aufbau des Moleküls nicht ganz, müsste Schwefel nicht zwei freie Elektronenpaare haben, genau wie Sauerstoff?
Und was bedeuten die gestrichelten Linien, sind das auch Elektronenpaarbindungen?
Wenn ja, wie sind dann die Oktettregeln für die einzelnen Atome erfüllt (bei mir hat Schwefel hier 12 Elektronen ?!)
Und wie genau reagiert nun das Wasser damit , ist das eine Säure Base-Reaktion?
Bin hier echt raus.
Sorry für die vielen Fragen und danke schonmal für eure Antworten.
1 Antwort
Bitte vergiss die Oktettregel für Schwefel wieder. Diese gilt nicht für Elemente jenseits der 2. Periode.
Schwefel hat Zugang zu weiteren orbitalen. Die gestrichelten Linien zeigen an, dass die tatsächlichen Bindungsverhältnisse irgendwo dazwischen sind.
Die negative Ladung ist somit über die vier Sauerstoffatome verteilt.
Dithionit reagiert mit Wasser und wird sich ein Proton oder auch mehr schnappen. (Hydrogensulfate etc).
Aso, okay, deshalb hat das Schwefel mehr.
Aber woher kommen jetzt die 2 überschüssigen Elektronen?