Kupfersulfid in elementare Bestandteile?
Hi, ich bin gerade dabei für eine Chemiklausur zu lernen.
Es geht um Redoxreaktionen, die ich eig super verstanden habe - soweit jedenfalls.
- Stelle die Redoxgleichung für die Verbrennung von Magnesium in Sauerstoff auf. Markiere Oxidation und Reduktion sowie Oxidationsmittel und Reduktionsmittel.
So weit so gut. Hab ich verstanden, gemacht und was ordentliches raus (siehe Bild).
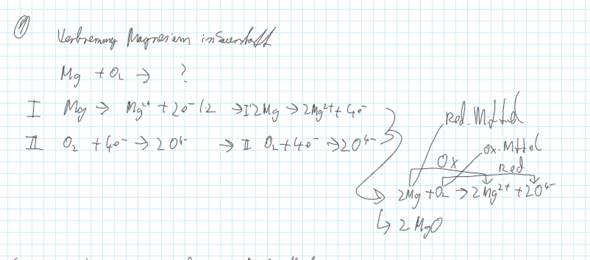
2 .
Kupfersulfid wird in seine elementaren Bestandteile zerlegt. Stelle die Reaktionsgleichung auf. Markiere Oxidation....
Wie mach ich das denn jetzt?
Als erstes habe ich versucht einfach nur ne Gleichung aufzustellen.
Hierbei habe ich dieses Video benutzt: https://www.youtube.com/watch?v=X9vV9JYQ_IM.
Bei mir kommt Cu²S³ raus (die 2 und 3 soll tiefgestellt sein).
Google ich das ganze jedoch ist die richtige Gleichung
2 Cu + S = Cu2S
Wieso denn 2 Cu?!
Außerdem, wie ist denn bitte der richtige Ansatz für die 2. Aufgabe?
1 Antwort

emm, Sauerstoff nimmt nur 2 Elektronen auf, also die beiden Atome aus O2 zusammen 4!
Wie kommst Du auf Cu3S2? Kupfer gibt ein oder zwei Elektronen ab. Außerdem sollst Du die AnalyseReaktion aufstellen!

Wäre zumindest eine Möglichkeit...
Ich mag ja Angaben zu Aggregatzuständen und Energien...
"emm, Sauerstoff nimmt nur 2 Elektronen auf, also die beiden Atome aus O2 zusammen 4!"
den feher hab ich korrigiert - danke!
wie würde denn eine analyse reaktion aussehen?
etwa so? https://www.bilder-upload.eu/bild-0a2c7f-1603557229.png.html