Fehlende Elektronenpaare von Valenzstrichformeln bestimmen?
Hallo ;),
Ich habe folgende Aufgabe gegeben: Wie viele Valenzelektronenpaare fehlen den jeweilligen Formeln, um die Struktur richtig zu beschreiben? Ladungen sind vollständig gegeben.
Ich gehe immer gleich vor und habe diesen Aufgabentyp meistens richtig, aber zum Beispiel bei den zwei Valenzstrichformeln habe ich ein anderes Ergebnis:
Ich schaue immer anhand des Periodensystems nach, wo die Elemente der Verbindung stehen und rechne die Valenzelektronen zusammen. Ich berücksichte dabei auch, ob die Verbindung Anionen bzw.Kationen hat und dann zähle ich die Valenzelektronen bei der Valenzstrichformel. Somit komm ich auf die fehlenden Elektronenpaare.
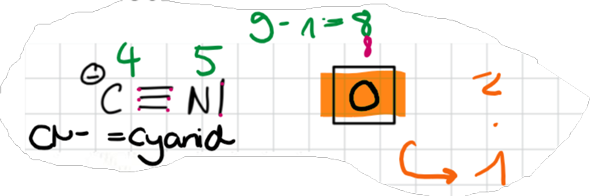
Bei Cyanid hätte man glaub ich +1 rechnen sollen. Aber das kann ich nicht nachvollziehen, weil Cyanid ja ein Anion besitzt.
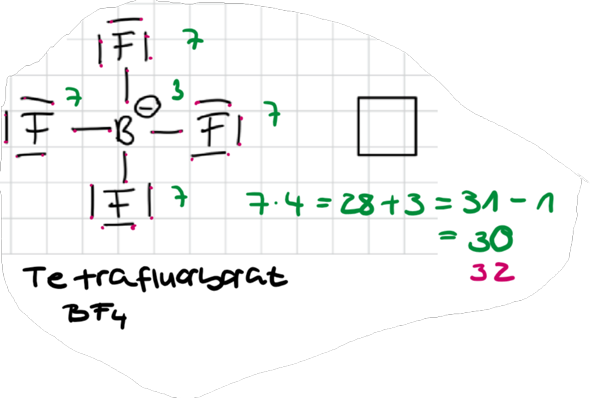
Bei Tetrafluorborat ist es genau das Gleiche.
Ich hoffe jemand kann mir weiterhelfen ;)
1 Antwort
Cyanid besitzt kein Anion, sondern es ist eins. Das stammt von der Blausäure HCN ab. Die verliert durch einen Säure-Base-Reaktion ein H+, übrig bleibt CN-. Um auf die Elektronen zu kommen, musst du jetzt natürlich +1 rechnen, weil C und N erstmal neutral sind. Die negative Ladung kommt ja von einem zusätzlichen Elektron. Wir haben also 4 Elektronen vom C, 5 vom N und eins vom H (das ja beim CN bleibt). Also insgesamt 10.
Beim BF4- genau dasselbe. Das kommt von der Tetrafluoroborsäure HBF4. Man kann es sich auch wie ein BF3 vorstellen, dem ein F- "aufgedrückt" wurde.
Ich hab das Bild oben wieder in meine Frage gepackt, weil ich es hier in dem Kommentar nicht einfügen konnte :)
Ja genau. Das Minus ist ja nur das Vorzeichen der Ladung und hat nichts mit dem Elektronenzählen zu tun, also nicht verwirren lassen
Vielen dank für deine Antwort! ;) Du hast es sehr gut erklärt. Das heißt ich schaue ob die Verbindung negativ geladen ist und addiere dann, anstatt zu subtrahieren. Also zum Beispiel bei Thiosulfat,da rechne ich auch +2 weil Thiosulfat zwei zusätzliche Elektronen hat (S2O32-) ?