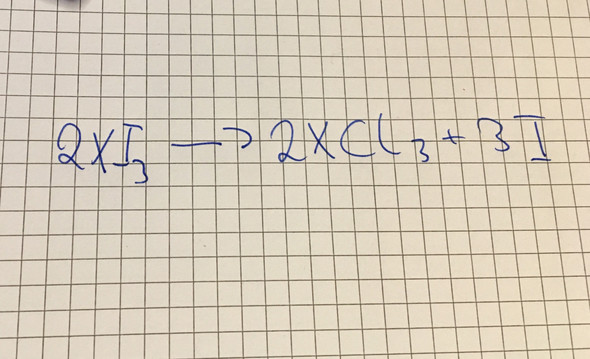Die Frage: Aus 12,5g Al/Mg Legierung erhalten wir 14, 34L H2 Gas bei T: 273,15K und p= 1,013bar. Wie viel Massenprozent hat Al in der Legierung. Ich habe mit der idealen Gaskonstanten begonnen und so die Stoffmenge von H2 bekommen.Die Idee ist anhand der Reaktionsgleichung (siehe Anhang) aber da häng ich irgendwie. Also in dem folgenden Bild habe ich mal alles zusammengefasst und mein Fortschritt ist auch zu sehen. Das Problem habe ich markiert.