Chemie Hilfe Note magnesium?
Wie kommt man von einem Magnesium Atom zum magnesium ion?
2 Antworten

Hi,
was hat eine Note mit einem Magnesium-Ion zu tun?
Stell dir mal Mg im Bohr'schen Atommodell vor. Drei Schalen, äußerste Schale hat zwei Elektronen auf der Außenschale (weil Mg in der zweiten Hauptgruppe steht).
Wir erinnern uns: Bei einer Art von Reaktionen werden Elektronen meist ausgetauscht, man spricht von einer Elektronenübertragungsreaktion. Das heißt, jemand gibt die Elektronen ab, ein anderer nimmt sie auf.
Bei Reaktionen versuchen die Elemente, ein Oktett auf der äußersten Schale zu haben (Aunahme: erste Periode). Das heißt, sie müssen Elektronen aufnehmen oder abgeben.
Wenn wir ein ungeladenes Atom haben, so stimmt die Anzahl der Elektronen mit der Anzahl der Protonen überein. Nun sagen wir, wir nehmen ein Elektron weg. Dann haben wir logischerweise ein Proton mehr, oder?
Wir sagen nun, wir haben Magnesium und wollen das Atommodell zeichnen, um uns das zu verdeutlichen. Dann schauen wir, wo Magnesium steht. Wir sehen: Zweite Hauptgruppe, dritte Periode. Das heißt Folgendes:
=> Das Atom hat zwei Elektronen auf der Außenschale (darüber gibt die Hauptgruppe Auskunft)
=> Das Atom hat drei Schalen, die mit Elektronen befüllt sind.
Weiterhin hat das Atom die Ordnungszahl 12. Das heißt, auf 3 Schalen müssen 12 Elektronen verteilt werden.
- wir wissen: Auf der äußersten Schale sind zwei Elektronen. Noch zehn elektronen gilt es zu verteilen.
- Auf der ersten Schale (von innen) sind nur zwei Elektronen. Denn da gibt es nur wasserstoff und Helium, weshalb Helium auch nur zwei Elektronen auf der Außenschale hat.
- Danach fängt die zweite Schale mit Kalium an. Wir haben zunächst ein Elektron auf der Außenschale. Wir passieren in der zweiten Periode noch sieben weitere Hauptgruppen, weshalb auf der vorletzten Schale acht Elektronen liegen müssen.
Es gibt noch Regeln für die Nebengruppenelemente etc, das lassen wir hier aber erstmal außer Acht.
Gehen wir einen Schritt weiter. Auf allen drei Schalen insgesamt haben wir 12 Elektronen, nicht wahr? Die Ordnungszahl ist gleich der Protonenzahl im Atomkern. Das heißt ja, dass wir zwölf Protonen haben und demnach auch zwölf Elektronen.
Nun nehmen wir ein Elektron weg. Was passiert? Logisch, wir haben elf Elektronen und zwölf Protonen. Wir haben also ein Proton im Überschuss! Also ist die Ladung einfach negativ. Vorher war das Atom ungeladen. Wir haben bisher also Mg+.
Nun ist aber auf der äußersten Schale (das Atommodell nach Bohr ist unten, damit du dir das vorstellen kannst) noch ein Elektron über - wir haben ja erst eines weg genommen. Jetzt müssen wir noch ein Elektron weg nehmen, um die volle Schale zu haben. Das Magnesium-Ion hat dann zwar nur zwei volle Schalen, aber das ist hier nicht so wichtig. Nun hast du also mg(2+), weil du zwei Protonen im Überschuss hast.
Ist dir das Prinzip klar? Wir erweitern das jetzt mal auf alle Hauptgruppen - bisher haben wir das ja nur für die zweite Hauptgruppe gemacht; das ist für alle Elemente der zweiten Hauptgruppe dasselbe, weil sie alle zwei Elektronen auf der Außenschale haben. Die Hauptgruppe gibt nämlich Auskunft über die Anzahl der Elektronen auf der Außenschale! Daraus folgt (nach dem gleichen Prinzip wie eben):
=> erste HG: gibt ein Elektron ab, also einfach positiv (z.B. Na+)
=> zweite HG: gibt zwei Elektronen ab, also zweifach positiv (z.B. Be 2+)
=> dritte HG: gibt drei Elektronen ab, also dreifach positiv (z.B. Al 3+)
=> vierte HG: gibt vier Elektronen ab oder vier Elektronen auf, also vierfach positiv oder negativ (kommt auf die Verbindung an, ob Elektronen abgegeben oder aufgenommen werden)
=> fünfte HG: nimmt drei Elektronen auf, also dreifach negativ (z.B. N 3-)
=> sechste HG: nimmt zwei Elektronen auf, also zweifach negativ (z.B. O 2-)
=> siebte HG: nimmt ein Elektron auf, also einfach negativ (z.B. Cl-)
Du schaust also, wie viele Elektronen das Element aufnehmen oder abgeben muss, damit es Edelgaskonfiguration erreicht. So nennt men den Zustand, wenn man eine volle AUßenschale hat. Diesen Zustand streben wie schon gesagt alle Elemente in einer Verbindung an.
Mehr gibt es dazu in meinen Augen auf der Ebene nicht zu sagen - bei Fragen melde dich.
LG
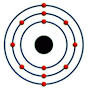

2 Elektronen wegnehmen --> mg2+