Hallo ;)
Ich habe eine Frage zur folgenden Aufgabe:
Wie ist der pH-Wert einer NH3/NH4+-Pufferlösung mit (NH4+)= 0,25 mol/L und (NH3)=0,55 mol/L?
Also eigentlich verstehe ich die Aufgabe, man muss ja einfach die Henderson-Haselbalch-Gleichung verwenden und die Wert von NH3 und NH4+ einsetzen. Und den pKS= 9, der in der Aufgabe a) schon gegeben wurde.
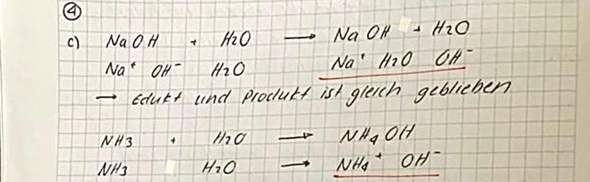
Aber ich verstehe nicht woran man erkennt was jetzt die Base und Säure ist.
In der Lösung ist NH3 die Base und NH4 die Säure. Aber warum?