Strukturformeln von unbekannten Stoffen bestimmen?
Hallo. Ich stelle mir die Frage, wie man Strukturformel von unbekannten Stoffen aufstellen kann. Als beispiel: Distickstoffmonoxid. Warum ist nicht das o atom in der Mitte. Woher weiß man, wie man die Atome anzuordnen hat, wenn nur der Name des Stoffs angegeben ist. GIbt es Tipps oder Regeln, wie sich manche Atome gerne verknüpfen ? Mir fällt dies oft ziemlich schwer. Danke für die Hilfe
3 Antworten

Warum ist nicht das o atom [sic] in der Mitte.
Weil man mit einem O-Atom in der Mitte keine Elektronenverteilung vornehmen kann, die die Bedingung erfüllt, dass alle beteiligten Atome über ein Elektronenoktett verfügen. Der Stickstoff hat 5 Valenzlektronen, der Sauerstoff hat 6. In der Summe sind das 16 Elektronen, die so verteilt werden müssen, dass alle Bindungspartner ein Elektronenoktett aufweisen. Wenn das O in der Mitte sitzt, sieht die Verteilung so aus:
IIN-OII-NII
Stelle dir die senkrechten Elektronenpaare (II) als waagerecht über die Elementsymbole geschrieben vor. Beim Sauerstoff sitzen dann korrekterweise 8 Elektronen, aber bei den Stickstoffen sind es jeweils nur 6. Anders ist es bei der Formel:
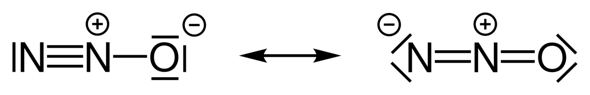
IN≡N⁺-OIII⁻
Hier haben alle Bindungspartner ein Elektronenoktett. Oder auch
IIN⁻=N⁺=OII
Die tatsächliche Formel ist also irgendwo dazwischen.


Du mußt Lewis-Formeln für beide Varianten aufstellen und dann auf Plausibilität überprüfen. Der wichtigste Punkt dabei sind die Formalladungen
- Für die unsymmetrische Anordnung bekommst Du N¯=N⁺=O und N≡N⁺–O¯ (die freien Elektronenpaare mußt Du Dir dazudenken weil ich sie hier nicht eintippen kann). Wir haben zwar Formalladungen (schlecht), aber nur einfache, und außerdem sind es zwei Grenzstrukturen (gut, Mesomeriestabilisierung).
- Die symmetrische Anordnung geht aber nur als N¯=O²⁺=N¯, und die doppelte positve Formalladung macht sie sehr unplausibel.

Ja. Du musst die Oktettregel anwenden.
Stickstoff hat demnach drei Bindungsplätze, Sauerstoff zwei.
Daraus folgt, dass Distickstoffmonoxid (Lachgas) ein Radikal ist, da die Oktettregel nicht erfüllt wird. Das Sauerstoffatom spaltet sich leicht ab, da Stickstoff mit sich selbst ein stabiles Molekül bildet.
Dann ist die Oktettregel auch wieder erfüllt.

Oh ja, danke! Das Wort ist mir nicht wirklich geläufig, wir sagten dem irgendwie anders. Nur weiss ich nicht mehr wie... 😅
*Oktettregel