Kann ich anhand der Säurekonstante ermitteln, in welchen Molmengen die Reaktionspartner in einer Säuredissoziation in Wasser vorliegen?
Angenommen ich habe eine 0,1 molare Ammonium-Lösung in Wasser. Der pKs von Ammonium ist 9,2.
Somit ist die Säurekonstante Ks von Ammonium 10^-9,2 mol/L
Wenn ich jetzt wissen möchte, zu wie viel Mol Hydronium-Ionen und wie viel Mol Ammoniak die 0,1 mol Ammonium in einem Liter Wasser dissoziieren, kann ich das dann mit diesen Angaben ermitteln?
Die Reaktion ist NH4++H2O⇌NH3+H3O+
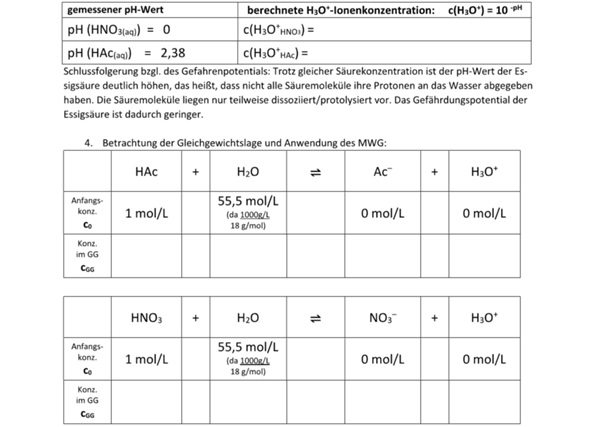
Das Massenwirkungsgesetz wäre hiermit:
Da jedes Hydronium-Ion mit der Bildung eines Ammoniakmoleküls einhergeht, ergibt sich bei bekannter Ammoniumkonzentration und bekannter Säurekonstante Ks: [H3O] wäre demnach 0,000007943282347 mol/L
Wenn aber von 0,1 mol/L Ammonium 0,000007943282347 mol/L zu Hydronium dissoziieren, dann liegen ja eigentlich nur 0,099992056 mol Ammonium vor. Ensprechend müsste im Massenwirkungsgesetz dann stehen:
Aber dann wäre das Ergebnis für [H3O] wiederum anders, mit 0,000007942966862 mol/L anstatt 0,000007943282347 mol/L.
Was mache ich falsch, bzw. wie werden die Konzentrationen der Reaktionspartner im Massenwirkungsgesetz bei gegebener Säurekonstanten und gegebener Ausgangskonzentration der Säure korrekt berechnet?
Mir ist bewusst, dass bei schwachsen Säuren dieser Unterschied in der Konzentration vor und nach Dissoziation vernachlässigt werden kann, da er sehr gering ist. Dennoch möchte ich es genau wissen. Und bei mittelstarken Säuren ist das wie ich meine auch ein echtes Problem.