Wie kann man sich eine Säurereaktion in Chemie vorstellen? Recht oberflächliche Verwirrung bitte um Erklärung ;) Chemie 10. Klasse?
Hey,
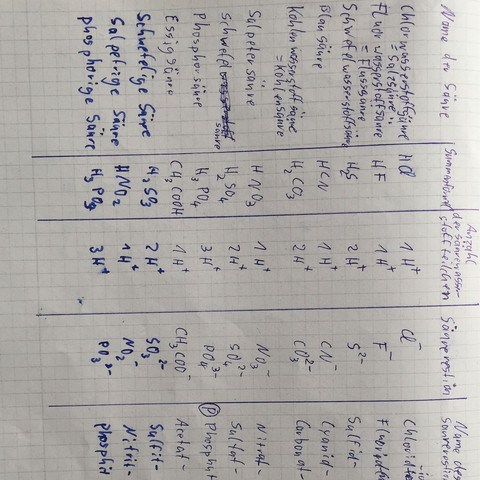
Ich hätte eine Frage zu Chemie und zwar haben wir als neues Thema jetzt Säuren und Basen und sind erstmal mit ein paar Säuren und einer Tabelle (siehe Anhang) eingestiegen. Nun aber meine Frage, wie kann man sich das mit den Anzahl der der Säurewasserstoffteilchen und dem Säurerestion vorstellen (also 3. und 4. Spalte)?
Also die Stoffe reagieren zu der Säure und was ist dann mit den Säurewasserstoffteilchen? Einfach aufschreiben wie viele das sind und da sie ja nur 1 Proton und kein Elektron besitzen ist es dann plus?
Und was genau ist der Säurerest? Darunter kann ich mir nichts vorstellen.
Wäre nett, wenn jemand vielleicht einfach kurz so einen Versuch darstellen kann und dann sagen kann, was der Säurerest und so weiter ist.
Danke und euch noch einen wunderschönes Wochenende!
LG
2 Antworten

Bei einer Reaktion gibt die Säure ein H+ ab und übergibt es an ein anderes Molekül, das in dem Fall als Base fungiert.
Ein einfaches Beispiel wäre die Reaktion von HCl (Salzsäure) mit Wasser. Wasser ist in dem Fall die Base (kann aber je nach Reaktionspartner als Säure oder als Base reagieren). Also gibt HCl sein einziges H+ ab und wird zu Cl-. Das Chloridion ist also der Säurerest. Gleichzeitig ist es die konjugierte Base der Salzsäure. Das abgegebene H+ schwirrt aber nicht einsam herum, sondern verbindet sich mit dem Wasser und bildet so H3O+. Das ist dann die konjugierte Säure von Wasser.
Wenn es sich um eine mehrprotonige Säure (eine Säure mit mehr als einem H) handelt, gibt sie die Protonen (also H+) nacheinander ab. Ein Beispiel wäre Schwefelsäure (H2SO4), die zuerst zu HSO4- (Hydrogensulfat) reagiert und dann, wenn das immer noch eine stärkere Säure als der Reaktionspartner ist, weiter zu SO42- (Sulfat).

Mit Lösen hat das nichts zu tun. Man kann z.B. sagen, man hat die Salzsäure mit Wasser umgesetzt.
Richtig, hinterher hat man wieder zwei verschiedene Stoffe. Bei einer Säure-Base-Reaktion findet immer nur ein Protonenübergang statt. Das bedeutet, dass lediglich das H+ von einer Verbindung auf eine andere übertragen wird.
Die Reaktionsgleichung zu der beschriebenen Reaktion wäre:
HCl + H2O --> Cl- + H3O+
Wird es so verständlicher?


Eine Säure gibt ein Proton ab. Oder eben auch mehr als nur Eines. Salzsäure als Beispiel hat die Summenformel HCl. Sie dissoziiert also in Lösung zu einem H+ und einem Cl- Ion.
H3PO4 hat aber jetzt 3 Wasserstoffe und gibt somit nach und nach diese ab. Dabei kommen also am Ende 3 H+ raus und übrig bleibt die konjugierte Base PO4(3-) als Anion.
Also hat man bei deinem Salzsäureversuch jetzt Salzsäure in Wasser gelöst? Und wir haben am Ende dann 2 verschiedene Stoffe (Cl und das wasser mit dem H)? Irgendwie blick ich da noch nicht so richtig durch. ;)