Ist die Messmethode zum Bestimmen der Konzentration einer schwachen Säure nicht super ungenau?
Wenn nach der Titration einer schwachen Säure nach Erreichen des Äquivalenzpunkts OH- Ionen übrig bleiben, dann bedeutet das doch, dass man mehr Moleküle der starken Base hinzugegeben hat, als ursprünglich schwache Säuremoleküle in der Lösung waren? wie will man so die Konz. der schwachen Säure ermitteln
2 Antworten

Wenn man mit einer pH-Elektrode titriert, dann sieht man ja die ganze Titrationskurve und kann den Äquivalenzpunkt aus der Kurve herausrechnen. Deine Meßserie liefert vielleicht Datenpunkte, die ungefähr so aussehen
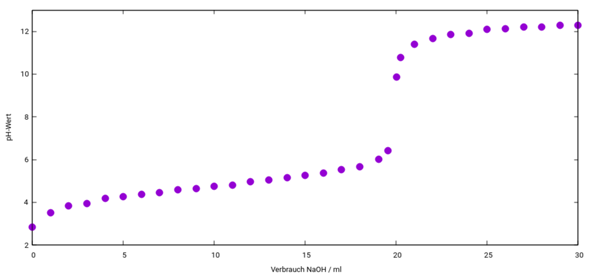
und dann kannst Du natürlich leicht eine Kurve hineinfitten, an deren Punkt der höchsten Steigung Du den Äquivalenzpunkt findest:
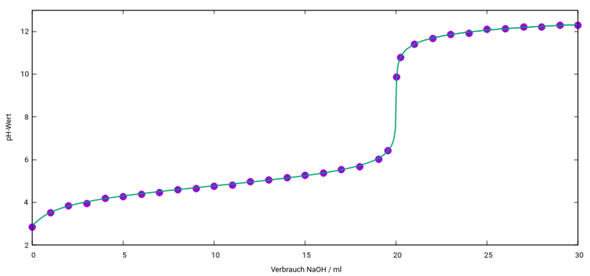
Wenn Du dagegen nach Großvaters Art mit pH-Indikator titrierst, dann hilft nur gute Arbeitstechnik: Mit Erfahrung merkt man beim Hineintropfen, ob die Titration bald am Ende ist, und reagiert darauf, indem man immer kleinere Volumina Maßlösung zutropft, in der Nähe des Äquivalenzpunktes nur noch einzelne Tropfen oder sogar halbe Tropfen. Auch das geht sehr genau, wenn man es anständig gelernt und geübt hat.
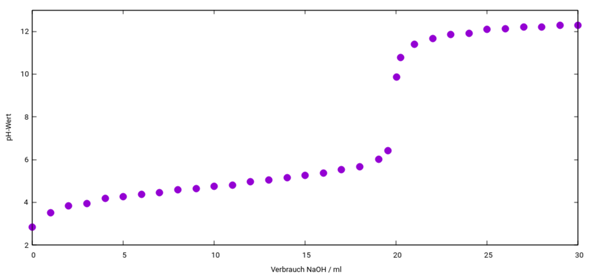
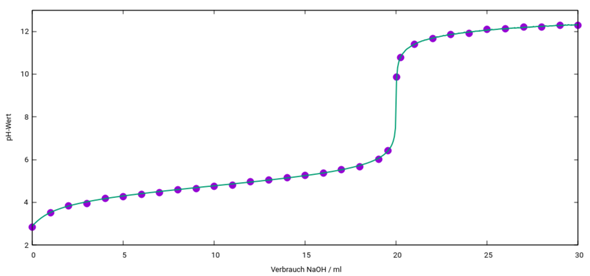


Tja, wenn man nicht sorgfältig Tröppje für Tröppje titriert, dann kann es natürlich vorkommen, dass man den Äquivalenzpunkt nicht genau genug erkennt. Zur sauberen Erkennung hat man schließlich einen geeigneten Indikator in der Brühe. Für die Titration von schwachen Säuren mit starken Basen verwendet man häufig Phenolphthalein, welches im Bereich von etwas über pH 8 von farblos nach violett umschlägt. Sobald der Farbumschlag nur langsam wieder verblasst, muss man sehr vorsichtig dosieren und an der Bürettenspitze anhaftende Basenlösung mit etwas dest. Wasser in die Vorlage spülen. Die ÄP ist erreicht, wenn die Farbe für vielleicht 20 Sekunden erhalten bleibt. Wenn der Ansatz einmal dunkel-violett bleibt, ist er übertitriert.

Auch das Einatmen größerer Mengen Wassers endet meist tödlich.
Phenolphtalein sollte man, wie andere Chemikalien auch, weder essen noch über die Pfoten schütten - das sollte auch Schülern bekannt sein, die alt genug sind fürs Chemielabor.

Die Existenz dieser H-Sätze ist ein Problem für den Einsatz in der Schule. Lösung muß unter 1% enthalten und darf nicht an der Schule hergestellt werden (auch nicht durch verdünnen).
H341 Kann vermutlich genetische Defekte verursachen
H350 Kann Krebs erzeugen
H361f Kann vermutlich die Fruchtbarkeit beeinträchtigen
Nein. Einen an der Spitze befindlichen Tropfen streift man an der Wand der Vorlage ab und spült ihn von dort ein.