Warum wird Zinn(II)-chlorid als ionisch betrachtet, sollte es nicht besser als Zinndichlorid bezeichnet werden?
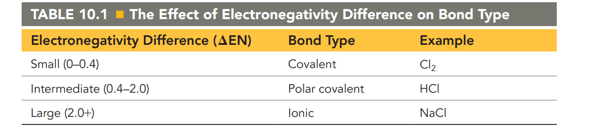
Ich habe gelernt, dass Bindungen als ionisch gelten, sobald der Ionencharakter etwa 50% beträgt, was bei einer Elektronegativitätsdifferenz ab 1,7 (oder ab 2 nach der untenstehenden Tabelle) der Fall ist.
In Zinn(II)-chlorid haben Sn und Cl jedoch nur einen Unterschied von 1,2, so dass ich die Benennung von Zinn(II) für Sn2+ und Chlorid für Cl- nicht verstehe, da das ja aussagt es seien Ionen.
(Chemistry: A Molecular Approach, Nivaldo J. Tro)
Ausgehend von dieser Einteilung müsste Zinn(II)-chlorid polar kovalent und nicht ionisch sein. Warum wird es dann nicht als Zinndichlorid bezeichnet?