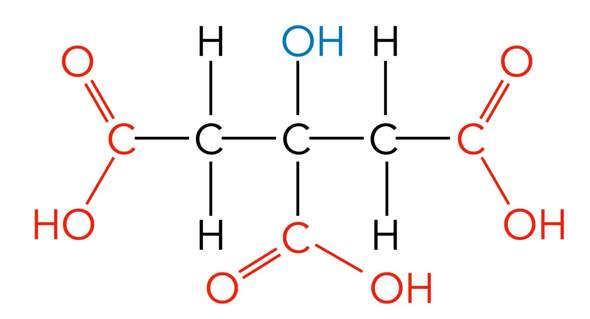
Warum lassen sich tertiäre Alkohol nicht mehr so leicht weiter oxidieren (z.B. Citrat)? Der Strich zum COO- könnte doch einfach umgelagert werden wenn COO-?
wenn COO- abgespalten wird?
Also ich versteh's so beim oxidieren eines sekundären Alkohols, dass zwei Wasserstoffatome gehen, sich abspalten und man daher eine Doppelbindung von Kohlenstoff und Sauerstoff erreicht. Wie bei 2-Propanol.
Wieso geht das bei Citrat nicht?
Man hat da an dem C-Atom wo das OH dranhängt zwar kein weiteres H-Atom mehr, aber man hat doch COO-
Wenn ich das COO- abspalte, dann kann ich doch einfach eine Doppelbindung zum C hinbekommen wenn das H-Atom am C auch abgespalten wird wie das COO-
In meinem Buch steht halt:
"Tertiäre Alkohole lassen sich nicht einfach so weiter oxidieren, da es kein freies Wasserstoffatom mehr gibt, das bei der Oxidation entfernt werden könnte"
Ja na und? Wieso kann man nicht das COO- analog zum H entfernen?