Was ist an meiner Ionenbildung falsch?
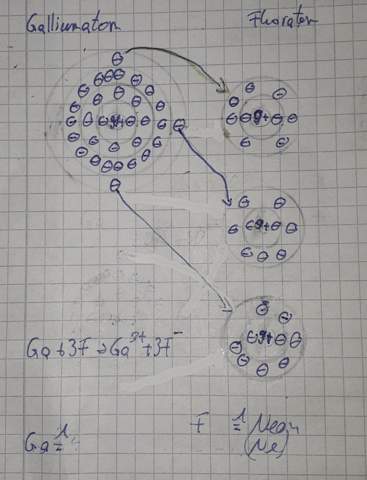
Ich soll als Hausaufgabe die Ionenbildung von Gallium mit Fluor skizzieren. Was ist an meiner Lösung falsch? Sie stimmt mit keinem Edelgas überein.
2 Antworten
Gallium erreicht durch die Abgabe von Elektronen KEINE Edelgaskonfiguration. Das können nur die Elemente links im PSE, indem sie Elektronen abgeben, und die rechts im PSE, indem sie Elektronen aufnehmen. Gallium steht aber rechts im PSE und gibt Elektronen ab. Mit links und rechts ist hier links und rechts der Übergangselemente gemeint.
Man könnte nun meinen, dass Gallium duch die Abgabe von 3 Elektronen die Konfiguration von Nickel erreicht, das hat ja 3 Elektronen weniger. Aber leider folgt die Abgabe von Elektronen anderen Regeln als die Auffüllug. Merke dir einfach, dass die Edelgasregel bei Übergangsmetallen und etwas rechts davon nicht gilt, oder nur mit Einschränkungen.
Es ist schon richtig, wie du es gezeichnet hast. Ga³⁺ hat 2 E. in der ersten, 8 E. in der zweiten und 18 E. in der dritten Schale. Die vierte Schale, die beim Kalium schon angefangen wird, wird bei der Bildung von Ga³⁺ wieder geleert. Verrückte Welt, oder wenn's einfach wär', könnt's jeder.
Fluor hat im Grundzustand (Atom) 7 Außenelektronen. Damit sind es 9 Elektronen insgesamt.
2+7 = 9
kommt noch eins vom Gallium hinzu, hat Fluor dann 8 Außenelektronen, also 10 gesamt.
2+7 + 1 = 10
Das entspricht dem Edelgas Neon.
da Fluor aber nur 1 Elektron aufnehmen kann, Gallium aber 3 abgeben möchte, musst du dann halt 3 Fluoratome mit Gallium verknüpfen zum Galliumfluorid GaF3.
Elektronenkonfiguration:
[Ar] 3d10 4s2 4p
OrbitalElektronen 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p1 4d0 4f0
Schalenmodell:
- 3 Elektronen in der äußersten besetzten Schale
- 18 Elektronen in der vorletzten besetzten Schale
- 8 Elektronen in der darunterliegenden besetzten Schale
Nein , die maximale Besetzung der inneren Schale mit 18 ist richtig. 2+6+10. Phoenix hat ganz genau hingeschribene
Gallium hat damit 4 Schalen, die erste hat 2 Elektronen, die nächste 8, die 3. 18 und die 4. noch 3
die 3. Schale mit 18 Elektronen liegt an der besonderen d-Orbital Konfiguration, die mehr als 8 Elektronen fassen kann, nämlich gezeigte 10. damit ist eine volle 3er Schale offiziell mit 18 Elektronen besetzbar.
dadurch entstehen die Nebengruppen mit den Halb- und den Edelmetallen.
Aber die Außenschale vom Gallium ist falsch. Da sind 18 drauf. Da es aber die Außenschale ist, passen nur 8 drauf